


生物技术进展 ›› 2024, Vol. 14 ›› Issue (1): 17-25.DOI: 10.19586/j.2095-2341.2023.0124
焦红燕1( ), 李国超1, 常亮1, 李岩异2, 翟丽丽1(
), 李国超1, 常亮1, 李岩异2, 翟丽丽1( )
)
收稿日期:2023-10-13
接受日期:2023-11-30
出版日期:2024-01-25
发布日期:2024-02-05
通讯作者:
翟丽丽
作者简介:焦红燕 E-mail:894808686@qq.com;
基金资助:
Hongyan JIAO1( ), Guochao LI1, Liang CHANG1, Yanyi LI2, Lili ZHAI1(
), Guochao LI1, Liang CHANG1, Yanyi LI2, Lili ZHAI1( )
)
Received:2023-10-13
Accepted:2023-11-30
Online:2024-01-25
Published:2024-02-05
Contact:
Lili ZHAI
摘要:
诺如病毒(norovirus,NoV)是引发急性胃肠炎疾病的主要病原体之一。NoV易发生突变产生多种毒株,对人类健康造成严重威胁。由于缺乏成功的动物模型,抗NoV药物和疫苗的后续评价受到了限制,目前尚没有上市的疫苗用于NoV的预防。对NoV疫苗的研究进展进行了综述,重点阐述了病毒样颗粒(virus like particles,VLP)疫苗、病毒载体疫苗和基于P颗粒疫苗的研究现状和发展前景,以期为NoV疫苗的研发提供新思路。
中图分类号:
焦红燕, 李国超, 常亮, 李岩异, 翟丽丽. 诺如病毒疫苗研究概况[J]. 生物技术进展, 2024, 14(1): 17-25.
Hongyan JIAO, Guochao LI, Liang CHANG, Yanyi LI, Lili ZHAI. Overview of Norovirus Vaccine Research[J]. Current Biotechnology, 2024, 14(1): 17-25.
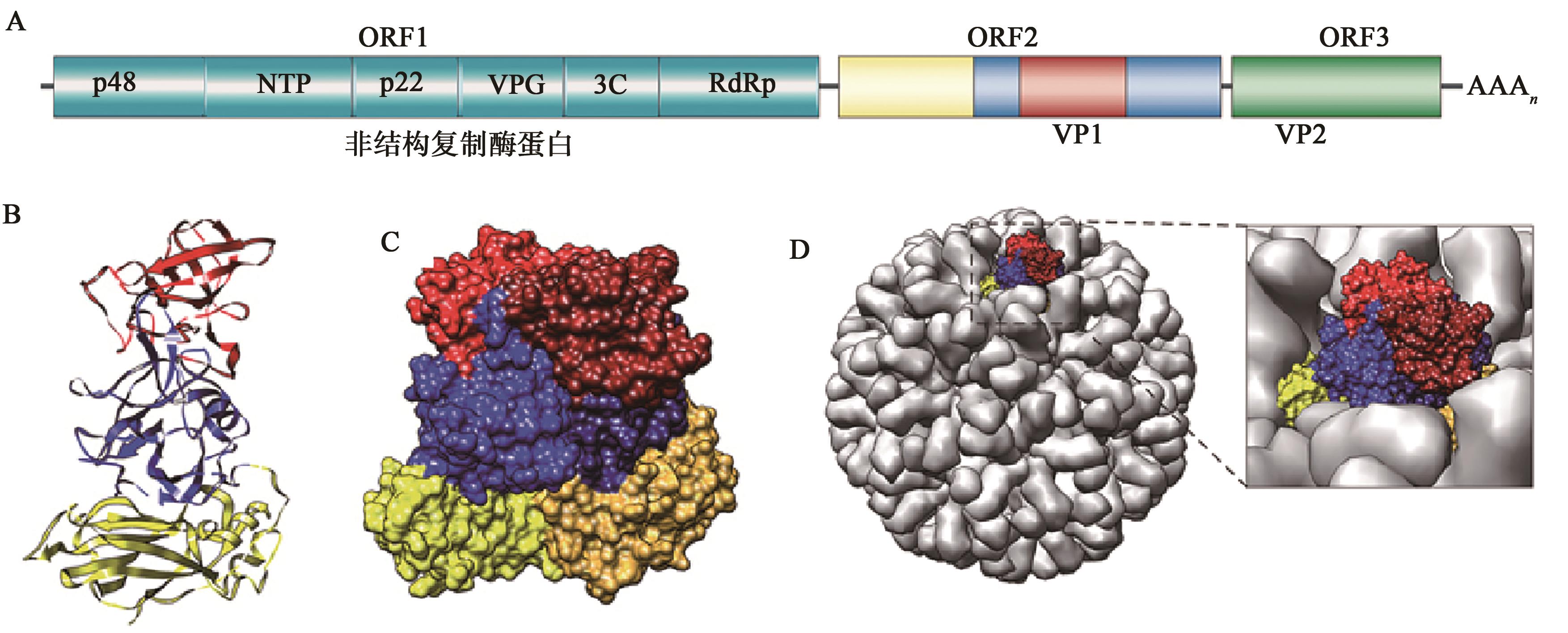
图1 NoV基因组及其衣壳结构[15]A:NoV基因组的线性结构。ORF1编码一个分子量为200 kD的多聚蛋白,后续被3C样蛋白酶切割为6个非结构蛋白(p48:分子量约48 kD;NTPase—核苷三磷酸酶,一种2C样蛋白;p22—分子量约22 kD,一种3A样蛋白;VPG—病毒基因组共价连接蛋白;3C—3C样蛋白酶;RdRp—RNA依赖的RNA聚合酶,一种3D样蛋白);ORF2全长1.8 kb,编码分子量为58 kD的主要衣壳蛋白VP1;ORF3编码次要结构蛋白VP2;B:VP1的单体结构。黄色为壳结构域,蓝色为P结构域的P1亚结构域,红色为P结构域的P2亚结构域;C:两个VP1单体形成A-B二聚体。浅色为A单体,深色为B单体;D:NoV VLP的完整结构。90个A-B二聚体从衣壳向外延伸,是受体结合区域和抗原变异位点。
Fig. 1 NoV genome and capsid structure[15]
| 疫苗类型 | 概念 | 优点 | 缺点 |
|---|---|---|---|
| 灭活疫苗 | 用物理、化学方法杀死病原微生物,但仍保持其免疫原性(能识别结合T/B细胞并使它们活化的能力)的一种生物制剂 | 安全性较高,疫苗稳定,易于保存 | 接种量大,需多次接种;只能引起体液免疫;免疫维持时间较短 |
减毒活疫苗 (活疫苗) | 活疫苗是通过毒力变异或人工选择法(如温度敏感株)而获得的减毒或无毒株,或者是从自然界直接选择出来的弱毒或无毒株经培养后制成的疫苗 | 接种量少,只需接种一次;可诱发体液和细胞免疫;免疫维持时间较长 | 有毒力回升的风险;疫苗不稳定,不易保存 |
| 亚单位疫苗 | 通过化学分解或有控制性的蛋白质水解方法,提取细菌、病毒的特殊蛋白质结构,筛选出具有免疫活性的片段制成的疫苗 | 减少了不良反应和疫苗引起的相关疾病 | 需要联合佐剂使用;不能诱发细胞和黏膜免疫 |
| 重组蛋白疫苗 | 将保护性抗原基因在真核或原核细胞体系中表达,并将其产生的蛋白抗原纯化后制成疫苗 | 安全性高,稳定性好,易放大生产 | 需使用佐剂,生产工艺复杂 |
| 病毒载体疫苗 | 将抗原基因插入病毒载体基因中,进入人体后使之高效表达抗原蛋白,进而诱发免疫保护作用 | 安全性高,可诱发体液和细胞免疫,载体可发挥佐剂作用 | 体内的预存免疫影响免疫效果 |
| RNA疫苗 | 体外合成编码目标抗原的mRNA序列,mRNA进入宿主细胞表达目标抗原从而激活免疫反应 | 安全性高,可快速制备,研发周期短 | 稳定性差,技术难度高,进入细胞效率低 |
| DNA疫苗 | 将含有抗原基因DNA序列的质粒直接引入人体,在宿主细胞内表达目标蛋白,激发机体产生免疫反应 | 生产周期短,可诱发体液和细胞免疫 | 免疫原性差,存在基因组整合突变风险 |
表1 疫苗类型[21]
Table 1 Types of vaccines[21]
| 疫苗类型 | 概念 | 优点 | 缺点 |
|---|---|---|---|
| 灭活疫苗 | 用物理、化学方法杀死病原微生物,但仍保持其免疫原性(能识别结合T/B细胞并使它们活化的能力)的一种生物制剂 | 安全性较高,疫苗稳定,易于保存 | 接种量大,需多次接种;只能引起体液免疫;免疫维持时间较短 |
减毒活疫苗 (活疫苗) | 活疫苗是通过毒力变异或人工选择法(如温度敏感株)而获得的减毒或无毒株,或者是从自然界直接选择出来的弱毒或无毒株经培养后制成的疫苗 | 接种量少,只需接种一次;可诱发体液和细胞免疫;免疫维持时间较长 | 有毒力回升的风险;疫苗不稳定,不易保存 |
| 亚单位疫苗 | 通过化学分解或有控制性的蛋白质水解方法,提取细菌、病毒的特殊蛋白质结构,筛选出具有免疫活性的片段制成的疫苗 | 减少了不良反应和疫苗引起的相关疾病 | 需要联合佐剂使用;不能诱发细胞和黏膜免疫 |
| 重组蛋白疫苗 | 将保护性抗原基因在真核或原核细胞体系中表达,并将其产生的蛋白抗原纯化后制成疫苗 | 安全性高,稳定性好,易放大生产 | 需使用佐剂,生产工艺复杂 |
| 病毒载体疫苗 | 将抗原基因插入病毒载体基因中,进入人体后使之高效表达抗原蛋白,进而诱发免疫保护作用 | 安全性高,可诱发体液和细胞免疫,载体可发挥佐剂作用 | 体内的预存免疫影响免疫效果 |
| RNA疫苗 | 体外合成编码目标抗原的mRNA序列,mRNA进入宿主细胞表达目标抗原从而激活免疫反应 | 安全性高,可快速制备,研发周期短 | 稳定性差,技术难度高,进入细胞效率低 |
| DNA疫苗 | 将含有抗原基因DNA序列的质粒直接引入人体,在宿主细胞内表达目标蛋白,激发机体产生免疫反应 | 生产周期短,可诱发体液和细胞免疫 | 免疫原性差,存在基因组整合突变风险 |
| 疫苗名称 | 疫苗类型 | 适应人群 | 开发公司 | 阶段 | 临床试验号 |
|---|---|---|---|---|---|
| HIL-214 | VLP重组蛋白 | 5个月婴儿 | 武田 | Ⅱ/Ⅲ期 | NCT05281094 |
| 四价重组诺如病毒疫苗(毕赤酵母) | VLP重组蛋白 | 6周婴儿、成人、老年人 | 安徽智飞 | Ⅰ/Ⅱ期 | NCT04563533 |
| VXA-NVV-201、VXA-NVV-202 | 腺病毒载体 | 18~49岁;18~80岁 | Vaxart | Ⅰ/Ⅱ期 Ⅱ期 | NCT05212168 NCT05626803 |
重组诺如病毒双价 (GⅠ.1/GⅡ.4)疫苗 (汉逊酵母) | VLP重组蛋白 | 6个月婴儿~59岁成人 6个月婴儿~13岁儿童 | 国药中生 | Ⅱ期 Ⅲ期 | NCT04941261 NCT05916326 |
| 诺如病毒GI.4 / GI.4二价VLP疫苗 | VLP重组蛋白 | 18~40岁 | Icon Genetics GmbH | Ⅰ期 | NCT05508178 |
| 重组六价诺如病毒疫苗(康华生物) | VLP重组蛋白 | 18~59岁 | 成都康华 | Ⅰ期 | NCT05805618 |
| mRNA-1403/ mRNA-1405多价诺如病毒疫苗 | mRNA | 18~80岁 | Moderna | Ⅰ期 | NCT05992935 |
| 四价重组诺如病毒疫苗(汉逊酵母) | VLP重组蛋白 | 6个月婴儿、成人 | 远大赛威 | Ⅰ期 | CXSL2300464 CXSL2300465 |
表2 全球处于临床研究的NoV疫苗
Table 2 NoV vaccines in clinical research worldwide
| 疫苗名称 | 疫苗类型 | 适应人群 | 开发公司 | 阶段 | 临床试验号 |
|---|---|---|---|---|---|
| HIL-214 | VLP重组蛋白 | 5个月婴儿 | 武田 | Ⅱ/Ⅲ期 | NCT05281094 |
| 四价重组诺如病毒疫苗(毕赤酵母) | VLP重组蛋白 | 6周婴儿、成人、老年人 | 安徽智飞 | Ⅰ/Ⅱ期 | NCT04563533 |
| VXA-NVV-201、VXA-NVV-202 | 腺病毒载体 | 18~49岁;18~80岁 | Vaxart | Ⅰ/Ⅱ期 Ⅱ期 | NCT05212168 NCT05626803 |
重组诺如病毒双价 (GⅠ.1/GⅡ.4)疫苗 (汉逊酵母) | VLP重组蛋白 | 6个月婴儿~59岁成人 6个月婴儿~13岁儿童 | 国药中生 | Ⅱ期 Ⅲ期 | NCT04941261 NCT05916326 |
| 诺如病毒GI.4 / GI.4二价VLP疫苗 | VLP重组蛋白 | 18~40岁 | Icon Genetics GmbH | Ⅰ期 | NCT05508178 |
| 重组六价诺如病毒疫苗(康华生物) | VLP重组蛋白 | 18~59岁 | 成都康华 | Ⅰ期 | NCT05805618 |
| mRNA-1403/ mRNA-1405多价诺如病毒疫苗 | mRNA | 18~80岁 | Moderna | Ⅰ期 | NCT05992935 |
| 四价重组诺如病毒疫苗(汉逊酵母) | VLP重组蛋白 | 6个月婴儿、成人 | 远大赛威 | Ⅰ期 | CXSL2300464 CXSL2300465 |
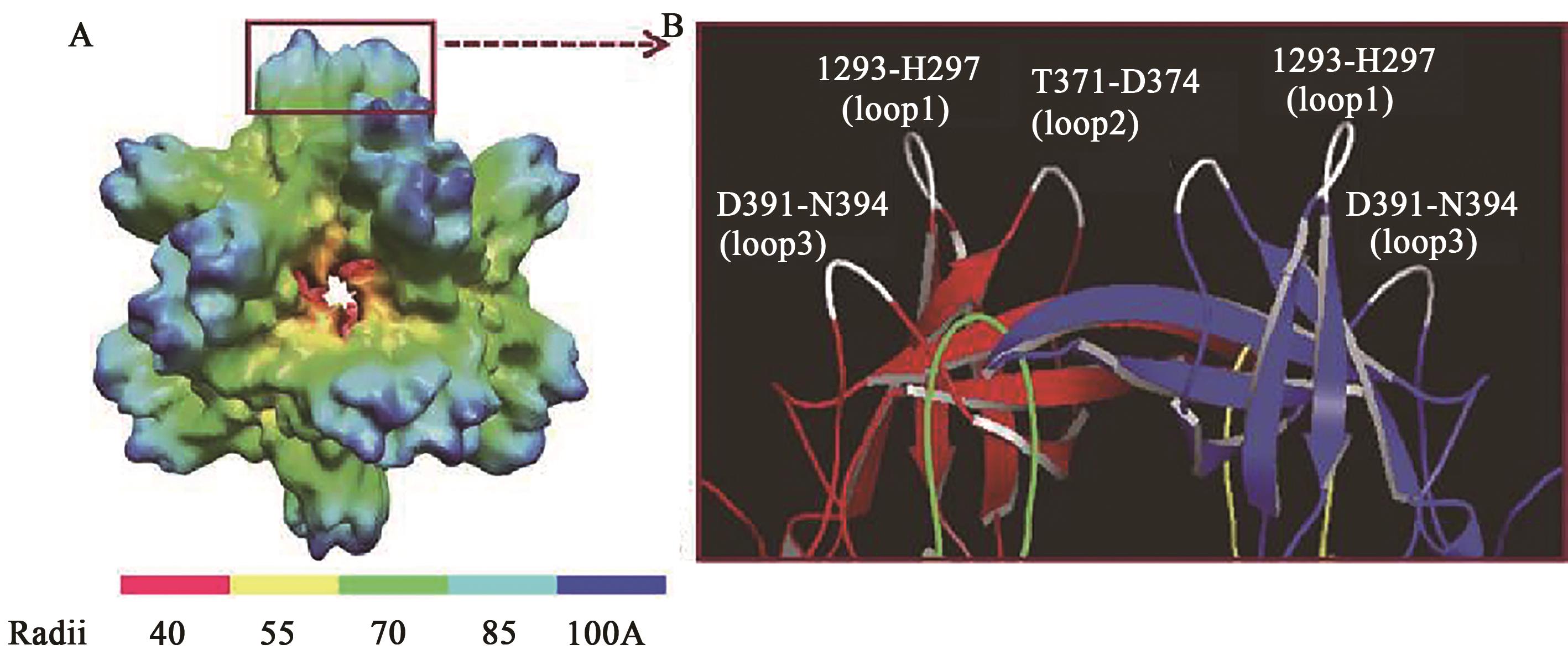
图3 NoV P颗粒及其表面环[49-50]A:VA387(GⅡ.4)NoV P颗粒结构的冷冻电镜重建图。P颗粒的半径用不同的颜色表示;B:P颗粒远端突出结构的晶体结构卡通模型图;其中,红色(P2结构域)和绿色(P1结构域)为一个P结构单体,蓝色(P2结构域)和黄色(P1结构域)为P二聚体的另一个P结构单体,白色为P2结构域的表面环。
Fig. 3 NoV P particles and their surface rings[49-50]
| 1 | 王金冬,马亚林,毛彤瑶,等.表达诺如病毒衣壳蛋白的重组腺病毒疫苗的构建及其免疫原性分析[J].中国生物制品学杂志,2022,35(3):257-262. |
| WANG J D, MA Y L, MAO T Y, et al.. Construction and immunogenicity of recombinant adenovirus vaccine expressing capsid protein of norovirus[J]. Chin. J. Biol., 2022, 35(3): 257-262. | |
| 2 | AHMED S M, HALL A J, ROBINSON A E, et al.. Global prevalence of norovirus in cases of gastroenteritis: a systematic review and meta-analysis[J]. Lancet Infect. Dis., 2014, 14(8): 725-730. |
| 3 | BARTSCH S M, LOPMAN B A, OZAWA S, et al.. Global economic burden of norovirus gastroenteritis[J/OL]. PLoS ONE, 2016, 11(4): e0151219[2023-12-07]. . |
| 4 | 刘宇阳,陈勇.诺如病毒疫苗的研究进展[J].微生物学免疫学进展,2020,48(4):46. |
| LIU Y Y, CHEN Y. Research progress of norovirus vaccine[J]. Prog. Microbiol. Immunol., 2020, 48(4): 46. | |
| 5 | 侯亚楠,李启明.诺如病毒及其疫苗研究进展[J].中华微生物学和免疫学杂志,2019,39(8):628-632. |
| HOU Y N, LI Q M. Progress in norovirus research and vaccine development[J]. Chin. J. Microbiol. Immunol., 2019, 39(8): 628-632. | |
| 6 | LUCERO Y, MATSON D O, ASHKENAZI S, et al.. Norovirus: facts and reflections from past, present, and future[J/OL]. Viruses, 2021, 13(12): 2399[2023-11-30]. . |
| 7 | 刘晖,周东明,谢迪,等.六价诺如病毒VLPs疫苗及其制备方法:CN115677838A[P].2023-02-03. |
| LIU H, ZHOU D M, XIE D, et al.. Hexavalent norovirus VLPs vaccine and its preparation method:CN115677838A[P].2023-02-03. | |
| 8 | ZHAO B, HU L, SONG Y, et al.. Norovirus protease structure and antivirals development[J/OL]. Viruses, 2021, 13(10): 2069[2023-11-30]. . |
| 9 | CAMPILLAY-VÉLIZ C P, CARVAJAL J J, AVELLANEDA A M, et al.. Human norovirus proteins: implications in the replicative cycle, pathogenesis, and the host immune response[J/OL]. Front. Immunol., 2020, 11: 961[2023-11-30]. . |
| 10 | VONGPUNSAWAD S, VENKATARAM P V, ESTES M K. Norwalk virus minor capsid protein VP2 associates within the VP1 shell domain[J]. J. Virol., 2013, 87(9): 4818-4825. |
| 11 | OPERARIO D J, PLATTS-MILLS J A, NADAN S, et al.. Etiology of severe acute watery diarrhea in children in the global rotavirus surveillance network using quantitative polymerase chain reaction[J]. J. Infect. Dis., 2017, 216(2): 220-227. |
| 12 | TAN M, HEGDE R S, JIANG X. The P domain of norovirus capsid protein forms dimer and binds to histo-blood group antigen receptors[J]. J. Virol., 2004, 78(12): 6233-6242. |
| 13 | ALLEN D J, GRAY J J, GALLIMORE C I, et al.. Analysis of amino acid variation in the P2 domain of the GII-4 norovirus VP1 protein reveals putative variant-specific epitopes[J/OL]. PLoS ONE, 2008, 3(1): e1485[2023-12-07]. . |
| 14 | YAO L, LI F, WANG L, et al.. Function of VP2 protein in the stability of the secondary structure of virus-like particles of genogroup Ⅱ norovirus at different pH levels: function of VP2 protein in the stability of NoV VLPs[J]. J. Microbiol., 2014, 52(11): 970-975. |
| 15 | DONALDSON E F, LINDESMITH L C, LOBUE A D, et al.. Viral shape-shifting: norovirus evasion of the human immune system[J]. Nat. Rev. Microbiol., 2010, 8(3): 231-241. |
| 16 | CHHABRA P, GRAAF M D, PARRA G I, et al.. Updated classification of norovirus genogroups and genotypes[J]. J. Gen. Virol., 2019, 100(10): 1393-1406. |
| 17 | DE GRAAF M, VAN BEEK J, KOOPMANS M P G. Human norovirus transmission and evolution in a changing world[J]. Nat. Rev. Microbiol., 2016, 14(7): 421-433. |
| 18 | 熊佩.诺如病毒四价疫苗的免疫学评价和GⅡ.4型诺如病毒阻断抗体表位的鉴定[D].上海:中国科学院大学(中国科学院上海巴斯德研究所),2019. |
| XIONG P. Immunological evaluation of Norovirus tetravalent vaccine and identification of GⅡ.4 Norovirus blocking antibody epitopes[D]. Shanghai: University of the Chinese Academy of Sciences (Chinese Academy of Sciences Shanghai Pasteur Institute), 2019. | |
| 19 | ZHENG D P, ANDO T, FANKHAUSER R L, et al.. Norovirus classification and proposed strain nomenclature[J]. Virology, 2006, 346(2): 312-323. |
| 20 | 杨洁.现代疫苗的发展、分类、影响因素及问题探讨[J].现代养生,2019,19(22):61-62. |
| YANG J. Development, classification, influencing factors and problems of modern vaccines[J]. Health Prot. Promot., 2019, 19(22): 61-62. | |
| 21 | 王传林,李明,吕新军.人用疫苗的分类及生产工艺[J].中华预防医学杂志,2020,54(9):1017-1025. |
| WANG C Y, LI M, LV X J. Classification and production process of human vaccine[J]. Chin. Prev. Med., 2020, 54(9): 1017-1025. | |
| 22 | 曹颖雯,罗奕熔,梁耀民,等.人诺如病毒体外培养体系研究进展[J].现代预防医学,2020,47(22):4151-4154. |
| CAO Y W, LUO Y R, LIANG Y M, et al.. Research progress of human norovirus culture system in vitro[J]. Mod. Prev. Med., 2020, 47(22): 4151-4154. | |
| 23 | JONES M K, WATANABE M, ZHU S, et al.. Enteric bacteria promote human and mouse norovirus infection of B cells[J]. Science, 2014, 346(6210): 755-759. |
| 24 | ETTAYEBI K, CRAWFORD S E, MURAKAMI K, et al.. Replication of human noroviruses in stem cell-derived human enteroids[J]. Science, 2016, 353(6306): 1387-1393. |
| 25 | 周弘璐,汪萱怡.诺如病毒在研疫苗及挑战[J].中国新药杂志,2019,28(21):2607-2611. |
| ZHOU H L, WANG X Y. Norovirus vaccines under development and challenges[J]. Chin. J. N. Drugs, 2019, 28(21): 2607-2611. | |
| 26 | PARK B J, JUNG S T, CHOI C S, et al.. Pathogenesis of human norovirus genogroup Ⅱ genotype 4 in post-weaning gnotobiotic pigs[J]. J. Microbiol. Biotechnol., 2018, 28(12): 2133-2140. |
| 27 | SOUZA M, AZEVEDO M S, JUNG K, et al.. Pathogenesis and immune responses in gnotobiotic calves after infection with the genogroup Ⅱ.4-HS66 strain of human norovirus[J]. J. Virol., 2008, 82(4): 1777-1786. |
| 28 | FUENMAYOR J, GÒDIA F, CERVERA L. Production of virus-like particles for vaccines[J]. N. Biotechnol., 2017, 39(Pt B): 174-180. |
| 29 | NOORAEI S, BAHRULOLUM H, HOSEINI Z S, et al.. Virus-like particles: preparation, immunogenicity and their roles as nanovaccines and drug nanocarriers[J/OL]. J. Nanobiotechnol., 2021, 19(1): 59[2023-12-07]. . |
| 30 | JEONG H, SEONG B L. Exploiting virus-like particles as innovative vaccines against emerging viral infections[J]. J. Microbiol., 2017, 55(3): 220-230. |
| 31 | LEE Y T, KO E J, LEE Y, et al.. Intranasal vaccination with M2e5x virus-like particles induces humoral and cellular immune responses conferring cross-protection against heterosubtypic influenza viruses[J/OL]. PLoS ONE, 2018, 13(1): e0190868[2023-12-07]. . |
| 32 | MOHSEN M O, GOMES A C, VOGEL M, et al.. Interaction of viral capsid-derived virus-like particles (VLPs) with the innate immune system[J/OL]. Vaccines, 2018, 6(3): 37[2023-11-30]. . |
| 33 | ROLDÃO A, MELLADO M C M, CASTILHO L R, et al.. Virus-like particles in vaccine development[J]. Expert Rev. Vaccines, 2010, 9(10): 1149-1176. |
| 34 | WU X, CHEN P, LIN H, et al.. Hepatitis E virus: current epidemiology and vaccine[J]. Hum. Vaccin. Immunother., 2016, 12(10): 2603-2610. |
| 35 | ZHU F C, ZHANG J, ZHANG X F, et al.. Efficacy and safety of a recombinant hepatitis E vaccine in healthy adults: a large-scale, randomised, double-blind placebo-controlled, phase 3 trial[J]. Lancet Lond. Engl., 2010, 376(9744): 895-902. |
| 36 | 马苏达 T, 舍伍德 J, 门德尔曼 P,等.诺如病毒疫苗配制品及方法:CN113453711A[P].2021-09-28. |
| MASUDA T, SHERWOOD J, MENDELMAN P, et al.. Norovirus vaccine formulations and methods: CN113453711A[P]. 2021-09-28. | |
| 37 | BERNSTEIN D I, ATMAR R L, LYON G M, et al.. Norovirus vaccine against experimental human GII.4 virus illness: a challenge study in healthy adults[J]. J. Infect. Dis., 2015, 211(6): 870-878. |
| 38 | LINDESMITH L C, FERRIS M T, MULLAN C W, et al.. Broad blockade antibody responses in human volunteers after immunization with a multivalent norovirus VLP candidate vaccine: immunological analyses from a phase I clinical trial[J/OL]. PLoS Med., 2015, 12(3): e1001807[2023-12-07]. . |
| 39 | 程博.诺如病毒四价疫苗获批进入临床研究[J].高科技与产业化,2019(7):71. |
| CHENG B. Norovirus tetravalent vaccine approved for clinical research[J]. High Tech. Industrialization, 2019(7): 71. | |
| 40 | KIM S H, CHEN S, JIANG X, et al.. Newcastle disease virus vector producing human norovirus-like particles induces serum, cellular, and mucosal immune responses in mice[J]. J. Virol., 2014, 88(17): 9718-9727. |
| 41 | KIM L, MARTINEZ C J, HODGSON K A, et al.. Systemic and mucosal immune responses following oral adenoviral delivery of influenza vaccine to the human intestine by radio controlled capsule[J/OL]. Sci. Rep., 2016, 6: 37295[2023-12-07]. . |
| 42 | KIM L, LIEBOWITZ D, LIN K, et al.. Safety and immunogenicity of an oral tablet norovirus vaccine, a phase I randomized, placebo-controlled trial[J/OL]. JCI Insight, 2018, 3(13): 121077[2023-12-07]. . |
| 43 | JOHNSON P C, MATHEWSON J J, DUPONT H L, et al.. Multiple-challenge study of host susceptibility to Norwalk gastroenteritis in US adults[J]. J. Infect. Dis., 1990, 161(1): 18-21. |
| 44 | HARRINGTON P R, YOUNT B, JOHNSTON R E, et al.. Systemic, mucosal, and heterotypic immune induction in mice inoculated with Venezuelan equine encephalitis replicons expressing norwalk virus-like particles[J]. J. Virol., 2002, 76(2): 730-742. |
| 45 | MA Y, LI J. Vesicular stomatitis virus as a vector to deliver virus-like particles of human norovirus: a new vaccine candidate against an important noncultivable virus[J]. J. Virol., 2011, 85(6): 2942-2952. |
| 46 | LICHTY B D, POWER A T, STOJDL D F, et al.. Vesicular stomatitis virus: re-inventing the bullet[J]. Trends Mol. Med., 2004, 10(5): 210-216. |
| 47 | BUKREYEV A, COLLINS P L. Newcastle disease virus as a vaccine vector for humans[J]. Curr. Opin. Mol. Ther., 2008, 10(1): 46-55. |
| 48 | KARIKÓ K, BUCKSTEIN M, NI H, et al.. Suppression of RNA recognition by toll-like receptors: the impact of nucleoside modification and the evolutionary origin of RNA[J]. Immunity, 2005, 23(2): 165-175. |
| 49 | TAN M, FANG P, CHACHIYO T, et al.. Noroviral P particle: structure, function and applications in virus-host interaction[J]. Virology, 2008, 382(1): 115-123. |
| 50 | TAN M, HUANG P, XIA M, et al.. Norovirus P particle, a novel platform for vaccine development and antibody production[J]. J. Virol., 2011, 85(2): 753-764. |
| 51 | TAN M, JIANG X. The p domain of norovirus capsid protein forms a subviral particle that binds to histo-blood group antigen receptors[J]. J. Virol., 2005, 79(22): 14017-14030. |
| 52 | 吴佳颖,许红梅.与P颗粒相关的诺如病毒疫苗研究进展[J].世界最新医学信息文摘,2021,21(105):146-147+150. |
| WU J Y, XU H M. Research progress on norovirus vaccines related to P particles[J]. Digest World Latest Med. Inf., 2021, 21(105): 146-147+150. | |
| 53 | TAN M, FANG P A, XIA M, et al.. Terminal modifications of norovirus P domain resulted in a new type of subviral particles, the small P particles[J]. Virology, 2011, 410(2): 345-352. |
| 54 | CAO S, LOU Z, TAN M, et al.. Structural basis for the recognition of blood group trisaccharides by norovirus[J]. J. Virol., 2007, 81(11): 5949-5957. |
| 55 | XIA M, TAN M, WEI C, et al.. A candidate dual vaccine against influenza and noroviruses[J]. Vaccine, 2011, 29(44): 7670-7677. |
| 56 | WANG L, CAO D, WEI C, et al.. A dual vaccine candidate against norovirus and hepatitis E virus[J]. Vaccine, 2014, 32(4): 445-452. |
| 57 | XIA M, WEI C, WANG L, et al.. A trivalent vaccine candidate against hepatitis E virus, norovirus, and astrovirus[J]. Vaccine, 2016, 34(7): 905-913. |
| 58 | YU Y, FU L, SHI Y, et al.. Elicitation of HIV-1 neutralizing antibodies by presentation of 4E10 and 10E8 epitopes on Norovirus P particles[J]. Immunol. Lett., 2015, 168(2): 271-278. |
| 59 | 付璐.基于诺如病毒P颗粒的Aβ免疫疗法对阿尔茨海默症的治疗效果研究[D].长春:吉林大学,2017. |
| FU L. Study on the effect of norovirus P particle-based Aβ immunotherapy of Alzheimer's disease[D]. Changchun: Jilin University, 2017. | |
| 60 | 孙瑶.以诺如病毒P颗粒为载体的pTau31表位疫苗对阿尔茨海默症的治疗研究[D].长春:吉林大学,2020. |
| SUN Y. Study on theimmunotherapeutic effect of a norovirus P particle-based pTau31 epitope vaccine for Alzheimer's disease[D]. Changchun: Jilin University, 2020. |
| [1] | 张鹏晓, 胡念. 黑色素瘤免疫治疗作用机制研究进展[J]. 生物技术进展, 2023, 13(6): 900-906. |
| [2] | 段平成, 郑凯, 张宇宏, 张国丽, 孙国清. 拮抗菌BJB01抗黄萎病的抗病效果评价[J]. 生物技术进展, 2023, 13(6): 913-918. |
| [3] | 张旭娟, 赵鹏翔, 刘子怡, 蔡子松, 刘梦昱, 谢飞, 马雪梅. EBV对宿主免疫的调控作用研究进展[J]. 生物技术进展, 2023, 13(5): 681-689. |
| [4] | 鲍佳生, 潘丙珍, 乔栖梧, 刘慧智, 潘素华. 酵母生物活性物质及其化妆品功效研究进展[J]. 生物技术进展, 2023, 13(3): 345-352. |
| [5] | 高宇轩, 靳静晨, 高雅娟, 张闻天, 李晨晨, 靳永胜. 异养硝化⁃好氧反硝化复合菌剂在垃圾渗滤液处理中的应用[J]. 生物技术进展, 2022, 12(4): 630-637. |
| 阅读次数 | ||||||
|
全文 |
|
|||||
|
摘要 |
|
|||||
版权所有 © 2021《生物技术进展》编辑部